Liệu pháp kháng sinh mới nhắm vào màng tế bào của vi khuẩn
Kháng kháng sinh là một vấn đề đang ngày càng trở nên phát triển hơn, ảnh hưởng đến sức khỏe cộng đồng toàn cầu. Trong đó, nhóm vi khuẩn gram âm đặc biệt khó điều trị, bởi vì các tế bào được che chắn bởi một lớp màng kép, tạo thành một rào cản bền vững đối với kháng sinh. Khi kháng sinh tiếp xúc với màng, những vi khuẩn này thường sử dụng kênh Efflux để loại bỏ thuốc. Gần đây, một số công bố các loại kháng sinh mới có khả năng vượt qua những trở ngại này bằng cách nhắm mục tiêu, trực tiếp hoặc gián tiếp lên một protein tích hợp vào màng tế bào.
Màng ngoài của vi khuẩn gram âm chứa các phân tử lipopolysaccharide (LPS) ở mặt phía bên ngoài của nó, với các protein màng ngoài (OMPs) bao quanh toàn bộ màng ngoài. Các OMPs được gấp vào màng bởi một phức hợp protein gọi là bộ máy lắp ráp β-barrel (BAM), thành phần trung tâm của nó là BamA, là một OMP. Do BamA tiếp xúc với không gian ngoại bào, nó có thể là một gót chân Achilles trong lá chắn vi khuẩn, khi đó chất ức chế truy cập BamA sẽ không cần phải xâm nhập vào tế bào. Thực tế, một nghiên cứu chứng minh cho luận điểm trên đã chỉ ra rằng phương pháp này ức chế sự gấp nếp của OMP và làm tổn hại đến tính toàn vẹn của màng theo một cơ chế chưa được biết rõ.
Nhà khoa học Imai và cộng sự đã phát hiện vi khuẩn gram âm sống cộng sinh trong ruột của giun tròn và chúng có thể tiết ra kháng sinh để chống lại vi khuẩn cạnh tranh – bao gồm cả các loài gram âm khác. Một lớp màng lọc của các chất tiết từ 22 trong số các loại vi khuẩn cộng sinh này đã cho thấy một loại kháng sinh có mục tiêu đến các nhóm vi khuẩn gram âm, được các nhà nghiên cứu đặt tên là darobactin.
Darobactin cho thấy hoạt tính kháng sinh chống lại nhiều vi khuẩn gram âm, cả trong điều kiện in vitro và ở chuột bị nhiễm bệnh, bao gồm cả một số mầm bệnh ở người bị kháng thuốc như Pseudomonas aeruginosa, Klebsiella pneumoniae và Escherichia coli. Darobactin không độc đối với tế bào người ở nồng độ kháng khuẩn hiệu quả của nó.
Các tác giả đã cung cấp bằng chứng cho thấy darobactin và BamA liên kết trực tiếp với nhau bằng cách sử dụng một kỹ thuật gọi là nhiệt lượng chuẩn độ đẳng nhiệt, đo lường sự thay đổi nhiệt liên quan đến tương tác vật lý giữa các phân tử. Kết quả của các thí nghiệm quang phổ cộng hưởng từ hạt nhân (NMR) cũng phù hợp với luận điểm liên kết trực tiếp và cho rằng kháng sinh ổn định các protein trong một cấu trúc có khả năng không hoạt động.
Cơ chế vượt qua màng tế bào kép
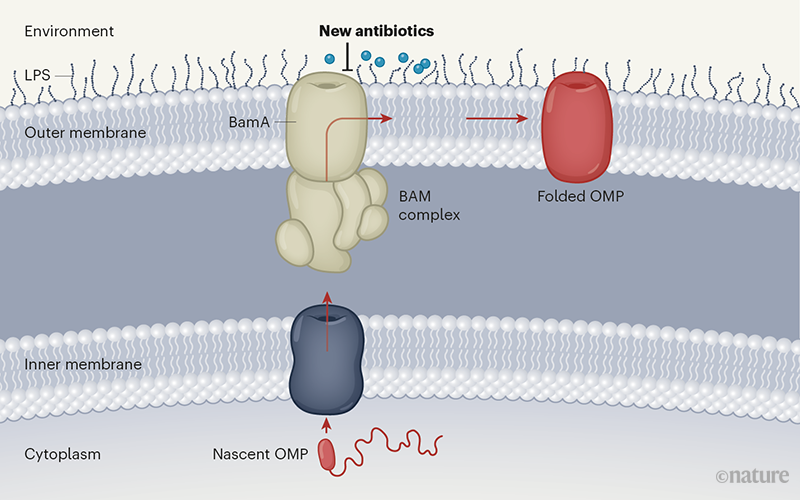
(Vi khuẩn gram âm được bảo vệ bởi màng trong và màng ngoài tế bào. Màng ngoài cấu thành từ các phân tử lipopolysaccharide (LPS) ở phía trong và liên kết với các OMPs. Các protein này được tổng hợp ở tế bào chất và chuyển đến gian bào bằng hệ thống vận chuyển nội bào. Tại đây, chúng được bắt, chèn và gập cuộn vào trong màng ngoài tế bào bằng phức hợp protein BAM. BamA là lõi của phức hợp BAM và tiếp xúc bề mặt vi khuẩn. Nhóm thuốc mới tập trung vào BamA để ngăn chặn sự gập cuộn bình thường của OMP, yếu tố cần thiết để vi khuẩn sống sót)
Theo Nature
Đỗ Trần Hương Duyên – Nguyễn Đức Huy, PTN Công nghệ enzyme và protein



